بهترین راه برای انتخاب بیمارانی که باید تحت درمان با Lu-177-PSMA (لوتشیوم-177) قرار گیرند که یک درمان رادیودارویی برای مداوای سرطان پروستات متاستاتیک تایید شده است، چیست؟ با توجه به مقالهای که اخیراً در نشست انجمن پرتوهای رونتگن آمریکا (ARRS) در نیواورلئان ارائه شد، معیارهای تصویربرداری میتوانند به انتخاب بهترین گزینه ها از میان بیماران، کمک کنند.
دکتر فیلیپ کو، از دانشگاه آریزونا در توسان، در نشست ARRS 2022 تحقیقی را ارائه نمود که در آن معیارهای جدیدی برای تصویربرداری در کارآزماییهای Lu-177-PSMA، درمان رادیولیگاندی بوسیله لوتشیوم-177 (Lu-177) آنتی ژن غشایی اختصاصی پروستات (PSMA) برای بیماران مبتلا به سرطان پروستات متاستاتیک، مد نظر قرار گرفته و بررسی شده است. او گفت: «این معیارها میتوانند راهنما و هدایتگر حرکتی رو به جلو برای پذیرفته شدن این رادیودارو به عنوان بخشی از فرایند مرسوم درمان باشد.»
وی افزود: «وقتی قصد ایجاد معیارهای تصویربرداری برای یک کارآزمایی بالینی را دارید، طبیعتاً میخواهید این کار را به گونهای انجام دهید که دارو مورد تایید قرار گرفته و در نهایت در زندگی واقعی قابل استفاده باشد.»
FDA رادیوداروی Lu-177-PSMA را تایید کرد. این رادیودارو در مارس 2022 برای درمان بیماران بزرگسال PSMA-مثبت مبتلا به سرطان پروستات متاستاتیک مقاوم به درمانهای معمول (mCRPC) (در این گونه از سرطان پروستات، بدن بیمار دیگر به هورمون درمانی جواب نمیدهد و سرطان در دیگر ارگانها و بافتهای بدن منتشر شده است) که قبلاً سایر درمانهای ضد سرطانی مانند درمان گیرنده آندروژن یا شیمی درمانی مبتنی بر تاکسان را دریافت کردهاند، به FDA ارائه شده بود.
FDA همچنین کیت تشخیصی ارائه شده را نیز تایید کرده است. از این کیت به منظور تهیه رادیوداروی Ga-68-PSMA به منظور شناسایی تومورهای متاستاتیک سرطان پروستات به وسیله تصویربرداری PET، استفاده میشود.
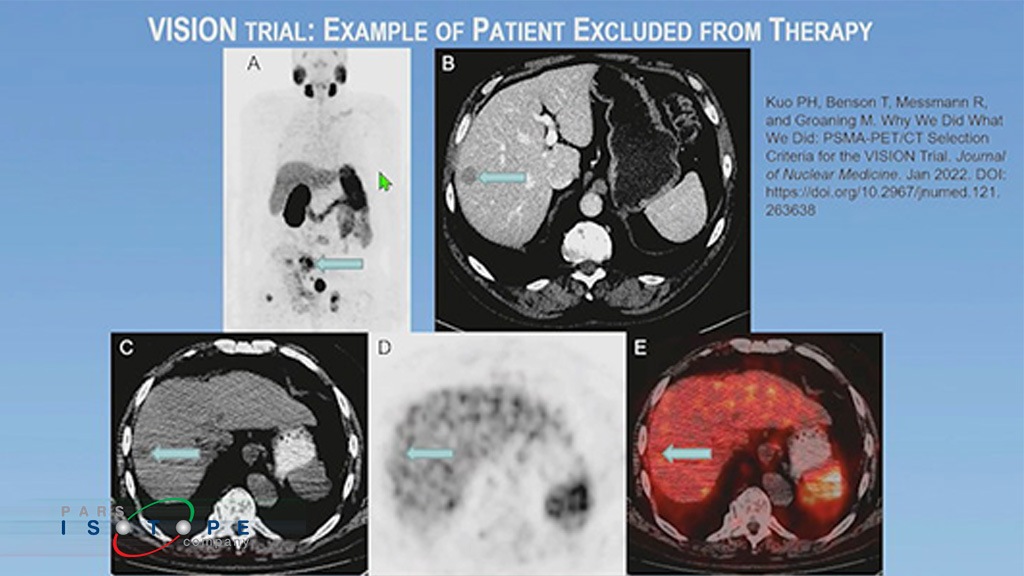
ابتدا، تعاریف جدیدی برای “PSMA-مثبت” و “PSMA-منفی” به طور خاص برای آزمایش VISION ایجاد شد. تعریف “PSMA-مثبت” نه برای تعیین مکان تجمع سلولهای سرطان پروستات، بلکه برای شناسایی تومورهایی با بیان کافی آنتی ژن غشایی اختصاصی پروستات به عنوان هدف که منجر به پاسخ به درمان خواهد شد، تعیین شده است.
کو گفت: «منظور ما از آنچه به عنوان یک ضایعه PSMA – مثبت در نظر گرفته میشود این نیست که فکر میکنیم سرطان پروستات است یا نه، بلکه این است که آیا فعالیت آن بیشتر از کبد است یا خیر.»
به گفته کو، چنانچه در بررسی بصری اسکن Ga-68-PSMA-PET/CT یک یا چند ضایعه در هر اندامی و با هر اندازه ای، با فعالیت جذبی بیشتر از کبد شناسایی شود، بیمار کاندیدای درمان خواهد بود.
او افزود که در کارآزمایی VISION، به دلیل تنوع SUV در سایتهای بالینی و چالشهای شناخته شده استانداردسازی، از روش تعیین یک مرز برای مقدار جذب استاندارد (SUV) استفاده نشد.
کو گفت: «مرحله بعدی کار، شامل بررسی اسکنهای CT و MRI برای شناسایی ضایعات بر اساس اندازه بود.»
معیارهای ارزیابی تصویربرداری آناتومیک به سه سیستم – غدد لنفاوی، اندامهای جامد (کبد، لوزالمعده، طحال و غدد فوق کلیوی – توخالی نیستند و بنابراین به عنوان اندامهای جامد شناخته می شوند.) و اسکلت – با معیارهای زیر تقسیم شدند:
- در صورتیکه عرض ضایعه (در محور کوتاه) 2.5 سانتی متر یا بزرگتر باشد، ارزیابی غدد لنفاوی انجام شود.
- برای متاستازهای پارانشیمی جامد، در صورتیکه عرض عارضه (در محور کوتاه) 1.0 سانتی متری یا بیشتر باشد، ارزیابی از نظر وضعیت PSMA انجام شود.
- متاستازهای استخوانی با یک جزء بافت نرم با عرض (در محور کوتاه) 1.0 سانتی متر یا بیشتر، و یا در صورتیکه تنها شامل بافت نرم باشند، مورد ارزیابی قرار گیرند.
چنانچه یکی از این معیارهای اندازه در سی تی اسکن بیمار مشاهده شود، ضایعههایی که دارای این معیارهای اندازه و نوع هستند، باید مورد ارزیابی قرار گیرند و اگر حتی یکی از آنها PSMA-منفی باشد، یعنی جذب مشابه یا کمتر از کبد داشته باشد، بیمار برای این درمان انتخاب نخواهد شد.
در این مطالعه در نهایت، حدود 15٪ از بیماران با توجه به معیارهای تصویربرداری ذکر شده از کارآزمایی VISION حذف شدند.
در مورد اثربخشی خود دارو، نویسندگان مقاله افزوده اند: «Lu-177-PSMA بقای کلی بیماران را در قیاس با استانداردهای مراقبت از 11.3 ماه به 15.3 ماه، بهبود بخشیده است.»
کو در پایان گفت: «شاید چهار ماه زیاد به نظر نرسد، اما برای این گروه از بیماران که بیماریشان به سرعت در حال پیشرفت است و شانس بقای ضعیفی دارند، این یک پیشرفت خوب محسوب میشود.»
منبع: Aunt Minnie